Metodevurderinger for retningslinjer – krefthandlingsplanene
Michael 2012;9: 183–195
Helse- og omsorgsdepartementet ga i 2005 Helsedirektoratet i samarbeid med regionale helseforetak og Nasjonalt kunnskapssenter for helsetjenesten (Kunnskapssenteret) i oppdrag å utarbeide nasjonale handlingsprogrammer for bedre kreftomsorg i Norge. Kreftstrategien inneholder nasjonale målsetninger/styringssignaler, planlagte/igangsatte tiltak og tiltak som skal vurderes – fordelt på kapitler om forebyggende arbeid, nasjonale screeningprogrammer, pasienten, helsetjenesten og samfunnet, diagnostikk, behandling, rehabilitering, lindrende (palliativ) behandling, personellfeltet, samt register- og forskningsvirksomheten. Samarbeidet tok utgangspunkt i arbeidet som så langt var drevet av de onkologiske faggruppene, og målet var å utforme retningslinjer, og å følge opp de nasjonale handlingsprogrammer på kreftområdet som skissert i Nasjonal helseplan. Bakgrunnen for oppdraget var at alle pasienter med kreft i Norge skal få likeverdig behandling av høy kvalitet. Handlingsprogrammene omfatter retningslinjer som setter nasjonal standard for kreftomsorgen, inkludert systemer for tidlig vurdering av ny diagnostikk og behandling innen kreftomsorgen. I de tilfeller hvor ny teknologi vil genere høye kostnader i helsetjenesten bør det gjøres helseøkonomiske analyser. Dette er avhengig av et tett og forpliktende samarbeid med fagmiljøene. Det formelle ansvaret for å utvikle de Nasjonale retningslinjene er lagt til Helsedirektoratet med bidrag i fra fagmiljøene. Kunnskapssenteret bidrar med medisinske metodevurderinger (HTA) som oppsummerer dokumenterte effekter av tiltaket, ofte med en fullstendig helseøkonomisk evaluering for å avklare kost-nytte for et helsetiltak det kan være tvil om skal inkluderes i nasjonale anbefalinger.
Bakgrunn
Likeverdighet og like muligheter er grunnleggende verdier i det norske samfunnet. Når sykdom inntreffer, skal ikke geografi eller sosial tilhørighet ha betydning for diagnostikk og behandling (1). Samtidig ser man også et stadig økende tilbud av ny og kostbar kreftbehandling, som har ført til oppslag i media og spørsmål i Stortinget om tiltak for å redusere forskjellene mellom landsdeler og sykehus (2). Tidligere utredninger har pekt på behovet for en samlet nasjonal strategi for kreftomsorgen, med handlingsplaner for hvordan de ulike utfordringene kan møtes. Dette ble realisert gjennom Nasjonal strategi for kreftområdet 2006–2009 (1).
Ansvaret for oppfølging av Nasjonal kreftstrategi ble gitt av Helse- og omsorgsdepartementet i 2005 til Helsedirektoratet i samarbeid med regionale helseforetak og Nasjonalt kunnskapssenter for helsetjenesten (Kunnskapssenteret) (1). Oppdraget var å utarbeide nasjonale handlingsprogrammer for kreftomsorgen i Norge, legge strategi for å møte fremtidige utfordringer på kreftområdet, legge til rette for bedre kvalitet og kompetanse, sikre tilstrekkelig kapasitet og likeverdig tilgjengelighet, hensiktsmessig organisering og bedre samhandling i og mellom alle ledd på kreftområdet (1, 3, 4).
Strategien inneholder nasjonale målsetninger og tiltak for hele kjeden inne kreftomsorgen:
Forebygging
Screening
Diagnostikk
Behandling
Rehabilitering
Lindrende behandling
Register- og forskningsvirksomheten
Tiltak for personellfeltet
Nasjonale handlingsprogrammer utgitt av Helsedirektoratet er å betrakte som retningsgivende anbefalinger, basert på oppdatert faglig kunnskap som er fremskaffet på en systematisk måte. De nasjonale retningslinjene gir uttrykk for hva som anses som god praksis på utgivelsestidspunktet, og er ment som et hjelpemiddel ved de avveininger tjenesteyterne må gjøre for å oppnå forsvarlighet og god kvalitet i tjenesten. Arbeidet skal bidra til at alle kreftpasienter i Norge skal få likeverdig behandling av høy kvalitet, og sette en nasjonal standard for kreftomsorgen. Et system for tidlig vurdering av ny og kostbar diagnostikk og behandling skal sikre at nye medikamenter og annen ny teknologi, for eksempel nye kirurgiske metoder, raskest mulig kan gjøres nasjonalt tilgjengelige i behandlingen av pasienter med kreft.
De tverrfaglige onkologiske miljøene har i en årrekke lagt ned et betydelig arbeid basert på at man i fagmiljøene har sett en klar nytte av en nasjonal konsensus omkring diagnostikk, behandling og oppfølgning. På denne måten utnytter man den nasjonale kompetansen istedenfor å legge dette ut på regionsnivå. Gjennom de siste 25 årene har man i disse fora utviklet faglige retningslinjer slik som «Grønnboka» for kolorektalkreft og «Blåboka» for brystkreft. Faggruppenes anbefalinger manglet imidlertid en offisiell status. Som ledd i Nasjonal strategi for kreftområdet (1) fikk Helsedirektoratet i oppdrag å videreutvikle og oppdatere faggruppenes anbefalinger til nasjonale handlingsprogrammer med retningslinjer for kreftbehandling. Ved å utarbeide nasjonale handlingsprogrammer samler man den ypperste kompetansen nasjonalt som man mener er den optimale måten å forbedre kvaliteten på i helsetjenesten samt å fremme en systematisk utvikling av klinisk praksis.
Helsedirektoratets rolle i utarbeidelse av handlingsprogrammene
Helsedirektoratet har både et koordinerende ansvar og et endelig ansvar for godkjenning av handlingsprogrammene (se figur). En egen stilling som strategidirektør ble opprettet i arbeidet med kreftstrategien. Dette har vært viktig, både for å ha et overordnet ansvar, sikre samkjøring mellom handlingsprogrammene, og for å sikre god kommunikasjon mot fagmiljøene. En styringsgruppe med representanter fra Helsedirektoratet, regionale helseforetak og Kunnskapssenteret ble opprettet for å følge arbeidet med kreftstrategien. Helsedirektoratet, ved strategidirektør og sekretariatet, prioriterer innkomne problemstillinger som de onkologiske faggruppene identifiserer i arbeidet, slik at Helsedirektoratet kan sende bestillinger på viktige metodevurderinger (HTA) til Kunnskapssenteret. Det er en omfattende prosess å lage gode retningslinjer som skal tilfredsstille krav til prosess, metode og transparens, og være på nivå med andre internasjonale organisasjoners utforming av anbefalinger og retningslinjer. Helsedirektoratets metodebok for nasjonale retningslinjer ligger til grunn for arbeid med handlingsprogrammene på kreftområdet (5). Arbeidet skal resultere i nasjonale handlingsprogrammer som er kunnskapsbaserte. Helsedirektoratet sender retningslinjene ut til høring til et samlet fagmiljø via RHF’ene før de godkjennes. Ved forslag til oppdatering av retningslinjene kontakter faggruppen Helsedirektoratet, og presenterer problemstillinger hvor det skal utarbeides metodevurderinger.
De regionale helseforetakene og de onkologiske faggruppene sin rolle i handlingsprogrammene
De regionale helseforetakene har ansvar for å foreslå fagpersoner til en onkologisk faggruppe som kan bistå i det konkrete arbeidet med handlingsprogrammene. Helsedirektoratet oppnevner så fagpersonene til å utarbeide og oppdatere nasjonale handlingsprogrammer for kreftomsorgen. De onkologiske faggruppene avklarer hva handlingsplanene bør omfatte innen diagnostikk, forebygging, primærbehandling og behandling av avansert sykdom. Faggruppene skriver så et utkast til handlingsprogram, med bistand fra Kunnskapssenteret til innhenting av litteratur, gradering av dokumentasjonsgrunnelaget og eventuelt utarbeidelse av nødvendige metodevurderinger. De regionale helseforetakene har ansvar for å implementere de offisielle nasjonale handlingsprogrammene på kreftområdet, og monitorere at behandlingen gis i henhold til gjeldende anbefalinger.
Kunnskapssenteretsrolle i utarbeidelse av handlingsprogrammene
Kunnskapssenteret har ansvar for å støtte Helsedirektoratet og faggruppene med god kunnskapshåndtering i utarbeidelsen av retningslinjene. Kunnskapssenteret bistår med metodestøtte, vurdering av studier og gradering av evidensen. Dette gjøres ved at Kunnskapssenteret søker etter retningslinjer, systematiske oversikter og eventuelt annen relevant litteratur. Gjennom disse søkene identifiserer Kunnskapssenteret faglig dokumentasjon som faggruppene bør bruke i retningslinjearbeidet. For enkelte spørsmål vil det ikke finnes tilstrekkelig oppdaterte, kunnskapsbaserte retningslinjer eller systematiske oversikter. Kunnskapssenteret kan da bistå faggruppene gjennom å utarbeide egne metodevurderinger. For noen spørsmål vil det være aktuelt med en kost-nytte vurdering, mens for andre vil helseeffektene være viktigst. Faggruppene må fremme behov for metodevurderinger til Helsedirektoratet, som har ansvar for å prioritere hvilke spørsmål som skal utredes og sende bestilling til Kunnskapssenteret. Det er et ønske at faggruppene skal bistå i å identifisere ny og kostbar behandling, slik at det tidlig kan foreligge en samlet vurdering av effekt og kost-nytte. En ny database for tidlig vurdering av ny diagnostikk og behandling er opprettet (www.mednytt.no), og denne gir oversikt over vurderinger av nye metoder som er utarbeidet av Kunnskapssenterets internasjonale samarbeidspartnere (6). Hensikten med databasen er å gi faglig støtte til helsepersonell og beslutningstakere når de skal vurdere om nye metoder skal innføres i helsetjenesten.
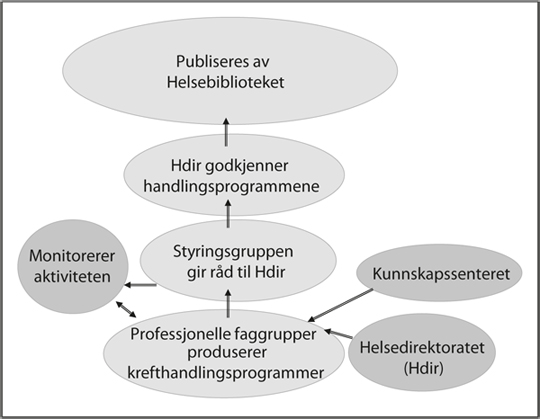
Figur. Prosess for utarbeidelse av nasjonale handlingsprogrammer for kreft.
De ferdige handlingsprogrammene publiseres på Helsebiblioteket (www.helsebiblioteket.no) og på hjemmesiden til Helsedirektoratet. Det er siden 2007 utarbeidet 11 nasjonale krefthandlingsplaner, hvor flere allerede er oppdatert. Flere handlingsprogrammer er under oppdatering, og nye handlingsprogrammer er under utarbeidelse. Totalt er det laget, eller er i arbeid, 22 handlingsprogrammer.
Nasjonalt handlingsprogram med retningslinjer for palliasjon i kreftomsorgen (2007, oppdatert 2010)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av nyrecellekreft (2007, under oppdatering)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av magekreft (2007)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av spiserørskreft (2007)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av tynntarmskreft (2007)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av brystkreft (2007, under oppdatering)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av maligne lymfomer (2008, oppdatert 2010)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av prostatakreft (2009, under oppdatering)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av kreft i tykktarm og endetarm (2010)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk behandling og oppfølging av testikkelkreft (2011)
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av maligne melanomer (2011)
Kunnskapsbaserte retningslinjer
En kunnskapsbasert retningslinje baserer seg på en standard som er utviklet gjennom AGREE-samarbeidet, og som er detaljert beskrevet i Helsedirektoratets metodebok for utarbeidelse av nasjonale retningslinjer (5). De nasjonale handlingsprogrammene for kreft baserer seg på de tidligere onkologiske faggruppenes retningslinjer, og vil ikke fullt ut ha en standard som tilfredstiller alle AGREE-kriteriene i de første versjonene. Men ved oppdateringer av handlingsprogrammene skal metodikken følges.
Systematiske søk
En viktig del av arbeidet med å utarbeide retningslinjer er å samle all den kunnskap som finnes innen det aktuelle området. Mengden av dokumentert kunnskap er stor, og arbeidet med å samle inn relevant dokumentasjon er omfattende. Søk bør derfor gjøres systematisk, og søkestrategien bør angis. Ulike spørsmål krever forskjellig dokumentasjon. For å vurdere effekten av tiltak, er det randomiserte kontrollerte studier en bør lete etter, mens det er prospektive kohortstudier som gir svar på spørsmål om risiko. Å lete etter systematiske oversikter eller solide internasjonale retningslinjer er første steg i arbeidet med å finne relevant dokumentasjon som grunnlag for nye retningslinjer. Det finnes mange elektroniske databaser over systematiske oversikter. The Cochrane Library er et eksempel på en slik kilde. Det er nødvendig å vurdere om de identifiserte systematiske oversiktene bygger på en tilfredsstillende metode. Kunnskapssenterets håndbok med sjekkliste for systematiske oversikter i vedlegg 1 benyttes for å undersøke dette (7).
Metodevurderinger
Kunnskapssenterets metodevurdering av et tiltak er en såkalt Health Technology Assessment (HTA) som vurderer klinisk effekt og sikkerhet, livskvalitet, organisasjon og økonomi. En metodevurdering er en systematisk oversikt over foreliggende dokumentasjon på et klart formulert forskningsspørsmål, hvor en bruker systematiske og eksplisitte metoder for å identifisere, velge, og kritisk vurdere relevant forskning, for så å samle inn og analysere data fra studiene som er inkludert i forskningsspørsmål. En systematisk oversikt baseres på felles internasjonale prinsipper (INAHTA checklist, Cochrane handbook) (7). Statistiske metoder (meta-analyse) kan, der det er mulig, brukes til å analysere og oppsummere resultatene fra de inkluderte studiene i et samlemål.
Helseøkonomiske vurderinger
Når en systematisk oversikt konkluderer med relativt presise effektestimater basert på rimelig gode studier, kan det være aktuelt å lage en helseøkonomisk analyse. Helseøkonomiske modeller estimerer ofte effekter som går over mange år, mens det kun finnes kliniske data fra en kortere tidsperiode. Da må det gjøres en del antakelser om effekten av helsetiltaket utover varigheten av den kliniske studien. Basert på tilgjengelige data for kostnader, nytte og risiko for ulike hendelser, lages en helseøkonomisk modell som brukes til å beregne kostnadeffekt-forhold (7). Fordelen med slike modeller er at vi kan gjøre sensitivitetsanalyser for å kartlegge hvordan resultatet påvirkes av endringer i forutsetningene som gjøres for variablene i modellen.
Resultatet av en slik analyse formuleres som kostnad per kvalitetsjustert leveår («gode leveår»), og kan dermed sammenlignes med andre tiltak innenfor samme eller andre terapiområder. Sensitivitetsanalysen kan også gi informasjon om et bestemt helsetiltak er kostnadseffektivt for noen pasientgrupper og ikke for andre. Det kan også være aktuelt å beregne de samfunnsøkonomiske kostnadene og de driftsøkonomiske kostnadene, og eventuelt beregne kostnader knyttet til den aktuelle sykdommen. I tilfeller der den kliniske effekten er usikker, kan det være aktuelt å gjøre en økonomisk evaluering som illustrerer konsekvensene av ulike, usikre effektestimater. Kunnskapssenteret følger en internasjonal metode for utarbeidelse av helseøkonomiske modellanalyser, og offentliggjør disse gjennom åpen publisering.
Tabell 1 viser hvilke metodevurderinger Kunnskapssenteret har gjort i forbindelse med utarbeidelsen av krefthandlingsplanene i Norge.
Nasjonalt råd for kvalitet og prioritering i helsetjenesten
I særlig utfordrene spørsmål om anbefalinger av helsetiltak kan Helsedirektoratet løfte spørsmålet til Nasjonalt råd for kvalitet og prioritering i helseog omsorgstjenesten (Rådet), og dette har hittil vært gjort fire ganger (se tabell 1). Rådet er sammensatt av medlemmer fra virksomheter med ansvar for helsetjenester, fra forvaltningen, fra brukerorganisasjoner og fra universiteter og høgskoler (8). Saker som kan være aktuelle for behandling i Rådet, er spørsmål knyttet til innføring av ny og kostbar teknologi/legemidler i sykehus og utvikling av nasjonale retningslinjer for å ivareta et likeverdig helsetilbud av god kvalitet.
Krefttype |
Tittel |
Vurderinger |
Rapport År |
Behandlet i Rådet |
|---|---|---|---|---|
Mange kreftformer |
Lindring av smerter hos pasienter med kreft |
Effekt Helseøkonomi (Organisatoriske, Etiske og Jurisdiske aspekter) |
Rapport fra Kunnskapssenteret nr. 09–2005 – HTA (metodevurdering) |
Nei |
Brystkreft |
Adjuvant behandling med trastuzumab ved tidlig stadium av brystkreft – en helseøkonomisk analyse |
Effekt Helseøkonomi |
August 2006 Rapport fra Kunnskapssenteret nr. 18–2006 |
Nei |
Kolorektalkreft |
Helseøkonomisk evaluering av bevacizumab ved metastatisk kolorektalcancer |
Effekt Helseøkonomi |
Desember 2007 Rapport fra Kunnskapssenteret nr. 23–2007 |
Ja |
Brystkreft Eggstokkreft |
Gentester for brystkreft og eggstokkreft |
Effekt Etikk |
Rapport fra Kunnskapssenteret nr. 05–2008 – Metodevurdering |
Ja |
Kolorektalkreft |
Oppsummering av publiserte helseøkonomiske evalueringer av cetuximab ved metastatisk kolorektalcancer |
Effekt Helseøkonomi |
Mai 2008 Rapport fra Kunnskapssenteret nr. 10–2008 |
Ja |
Mange kreftformer |
Sammenligning av palonosetron og ondansetron med hensyn på klinisk nytte og kostnad/effekt ved forebygging av kvalme og oppkast I forbindelse med kjemoterapi hos pasienter med kreft |
Effekt Helseøkonomi |
Juni 2008 Rapport fra Kunnskapssenteret nr. 18–2008 |
Nei |
Brystkreft |
Lapatinib ved avansert eller metastatisk HER-2 positiv brystkreft |
Effekt |
Metodevarsel 2008. Nr 1, januar 2008, fra MedNytt |
Nei |
Brystkreft |
Bevacizumab i førstelinjebehandling ved metastatisk brystkreft. |
Effekt |
Metodevarsel 2008. Nr. 2, juni 2008, fra MedNytt |
Nei |
Kolorektalkreft |
Screening av kolorektal kreft – effekt på dødelighet og forekomst. Oversikt over dokumentasjon og internasjonale anbefalinger |
Effekt |
Desember 2008 Rapport fra Kunnskapssenteret nr. 30–2008 |
Nei |
Brystkreft |
Helseøkonomisk analyse av bevacizumab+paclitaxel sammenlignet med paclitaxel alene om førstelinjebehandling ved metastatisk brystkreft |
Effekt Helseøkonomi |
April 2009 Rapport fra Kunnskapssenteret nr. 5–2009 |
Nei |
Palliasjon |
Metylnaltrekson (Relistor) ved obstipasjon i kreftbehandling |
Effekt Helseøkonomi |
September 2009 Rapport fra Kunnskapssenteret nr. 23–2009 |
Nei |
Mange kreftformer |
Estimering av behovet for PET/CT i 2020 |
Effekt Behovsestimering |
Notat 2009 – Hurtigoversikt |
Ja |
Lungekreft |
Klinisk nytte av PET integrert med CT for ikke-småcellet lungekreft |
Effekt |
Metodevarsel nr. 03–2010 |
Nei |
Kolorektalkreft |
Forventede virkninger ved innføring av screening for kolorektal kreft i Norge |
Effekt |
Notat 2010 – Hurtigoversikt |
Ja |
Kolorektalkreft |
Resultater fra kliniske effektstudier av screening for kolorektal kreft: hurtigoversikt |
Effekt |
Notat 2010 – Hurtigoversikt |
Ja |
I 2008 ble spørsmålet om ny medikamentell behandling av kolorektalkreft drøftet i Rådet. Et flertall av Rådet støttet forslaget om at, hvis man fortsatt skulle tilby denne behandlingen, måtte dette skje ved at man registrerte data om bruk innenfor rammen av en klinisk registerstudie (9). En slik studie vil kunne gi mulighet til å følge opp effekt og bivirkninger av behandlingen samt gi data for en re-evaluering av kostnadseffektivitet. Andre saker som har vært til drøfting i rådet er; gentester for brystkreft og eggstokkreft, behovet for PET-CT i 2020 og screening for kolorektalkreft (tabell 1). Sakene som blir behandlet i Rådet er retningsgivende for utarbeidelsen av alle krefthandlingsplanene.
Forts. neste side.
Anbefalingene skal være tydelige og dokumentasjonsgrunnlaget skal være synlig i handlingsprogrammene.
Vurdering av effekt og sikkerhet er vesentlig, men ikke alltid tilstrekkelig for å kunne gi en konkret anbefaling. Anbefalingene i handlingsprogrammet er evidensbaserte når de har en klar og tydelig ordbruk, og det er enkelt å koble anbefalingene til dokumentasjonen den bygger på. Jo klarere en anbefaling er, jo enklere og viktigere er det for helsepersonell å følge den. Effekten skal også sees i sammenheng med tilgjengelige ressurser. Metodevurderinger med helseøkonomiske analyser vil svare på om det er usikkert om nytten står i forhold til kostnadene.
For nye behandlingstiltak er det internasjonalt akseptert at de bør kunne vise til effekt i randomiserte kontrollerte studier. Det er derfor et mål å beskrive studiene som utgjør dokumentasjonsgrunnlaget. For mer etablerte tiltak kan en ikke forvente at det finnes dokumentasjonen på det samme nivået.
Generelt ser en at økninger i kostnadene for helsetjenester ofte er drevet av innovasjon (10). Innen kreftomsorgen tar innovasjonen mange former, inkludert nye tilnærminger til tidlig oppdagelse, nye medikamenter eller etablerte medikamenter til nye indikasjoner, nye kirurgiske metoder og utstyr, nye metoder for å levere strålebehandlinger, eller nye teknologier for å diagnostisere og overvåke pasienter. Begeistring for nye diagnostiske og terapeutiske metoder kan ha mange positive virkninger for pasientene, men klinikere og ledere i sykehus erfarer også at nye metoder i en del tilfeller innføres uten at effekt eller sikkerhet ved metodene er tilstrekkelig vurdert på forhånd. For legemidler har en et veletablert internasjonalt system for innføring, mens for annen ny teknologi finnes det foreløpig ikke tilsvarende systemer. Ett nytt system for innføring av ny teknologi er i startfasen i Norge (11), og arbeidet med handlingsprogrammer innen kreftområdet har vært en mal for et slikt system.
Det finnes mange systemer for å gradere dokumentasjonen i en retningslinje. Graderingen skal synliggjøre hvor godt dokumentert grunnlaget for anbefalingene er. I handlingsprogrammene skal det knyttes en bokstavverdi [A, B, C, D] til hver anbefaling som sier noe om hvilket dokumentasjonsgrunnlag anbefalingen er basert på. Dette systemet for gradering legger vekt på hvilken type studier som er gjennomført, og ikke hvilke dokumenterte helseeffekter som er grunnlag for anbefalingen. Dokumentasjonsgrunnlaget for anbefalingene vil derfor variere mye i handlingsprogammene. Noen anbefalinger vil være basert på meta-analyser som viser effekt på klinisk viktige utfallsmål (f. eks. overlevelse), andre anbefalinger vil være basert på enkeltstudier som kun viser effekt på surrogate utfallsmål (f. eks. sykdomsfri overlevelse, symptomkontroll eller livskvalitet). Noen studier vil ha flere effektmål som eventuelt kan vurderes samlet. Andre anbefalinger baserer seg hovedsakelig på klinisk erfaring.
Internasjonalt har et nytt system for gradering av kunnskapsgrunnlaget tatt over for flere av de tidligere systemene som kun la vekt på hvilken type studier som var gjennomført. Det nye graderingssystemet GRADE er et mer omfattende system for gradering, som graderer dokumentasjonen for relevante utfalsmål (12). Helsedirektoratets metodebok (5) gir følgende anbefaling om bruk av GRADE; Etter hvert som GRADE blir mer etablert og utbredt, vil behovet for flere system bli mindre. I utgangspunktet skal en bruke GRADE med mindre en vesentlig del av bakgrunnsmaterialet for retningslinjen har brukt et annet system. I krefthandlingsprogrammene vil det være aktuelt å benytte GRADE først og fremst i forbindelse med oppdatering av nye kostbare tiltak som vurderes tatt inn i handlingsplanene.
Fremtidige utfordringer
Kreftområdet er et fagområde med stor forskningsaktivitet, og behov for regelmessig oppdatering av retningslinjene. Tabell 2 viser forskningsaktiviteten som nå er registeret på kreftområdet i WHOs database over kliniske studier. Noe av denne forskningen vil gi resultater som får betydning for pasientbehandlingen. Årlig publiseres nesten 7000 kliniske studier, 3000 systematiske oversikter og nærmere 300 retningslinjer, informasjon som er relevant i arbeidet med å utforme retningslinjene.
Samtidig som tilbudet av nye metoder i kreftbehandlingen synes å øke, stiller myndighetene nå tydelige krav om å utrede kliniske effekter og kostnadseffektivitet før beslutninger tas. For mange nye teknologier vil man ha et begrenset kunnskapsgrunnlag som gjør det utfordrende å utføre gode helseøkonomiske analyser. Ny teknologi medfører «ringvirkninger» i systemet, hvor noen kan være kostnadsbesparende og andre kan være kostnadsøkende. Dette gir utfordringer når beslutninger skal tas basert på ett begrenset kunnskapsgrunnlag. Det stiller igjen krav til en tydelig organisering av arbeidet, tidlig identifisering av potensielle gjennombrudd, og effektiv utredningskompetanse. Det nylig etablerte forskningsprogrammet for offentlig initierte kliniske studier på kreftområdet hvor Norges forskningsråd og Kunnskapssenteret samarbeider basert på prioriteringer i Rådet, viser at Norge vil være med å bidra til at nødvendig ny kunnskap genereres på dette feltet.
Antall totalt |
Antall registrert i 2010 |
|
|---|---|---|
Pågående kliniske studier |
7337 |
|
Publiserte kliniske studier |
101527 |
6939 |
Systematiske oversikter |
38527 |
3238 |
Retningslinjer |
2325 |
288 |
Kliniske studier ble identifisert ved søk WHO portalen (http://apps.who.int/trialsearch/). Publiserte studier, systematiske oversikter og retningslinjer ble identifisert ved søk i Pubmed med følgende termer: Cancer or Neoplasm (Mesh) avgrenset til «systematic reveiws or metaanalysis», clinical trial or RCT, practice guideline.
Litteratur
Sosial og helsedepartementet. Nasjonal strategi for kreftområdet. Sosial- og helsedepartementet. Rundskriv 15.05.2006. http://www.regjeringen.no/upload/kilde/hod/prm/2006/0083/ddd/pdfv/292402-nasjonal_helseplan_saertrykk.pdf. Sosial og helsedepartementet, 2006.
Interpellasjon fra Laila Dåvøy (KrF) til helse- og omsorgsministeren. Om å sikre likebehandling av kreftpasienter, med henvisning til store forskjeller landsdeler og sykehus imellom. 31.03.2006. http://www.stortinget.no/no/Saker-og-publikasjoner/Sporsmal/Interpellasjoner/Interpellasjon/?qid=34257
Norges offentlige utredninger. Omsorg og kunnskap! Norsk kreftplan. NOU 1997: 20. Oslo: Statens forvaltningstjeneste.
Nasjonal strategi for arbeid innenfor kreftomsorgen. Kvalitet, kompetanse og kapasitet. Oslo: Helse og omsorgsdepartementet, 2004.
Helsedierktoratet. Retningslinjer for retningslinjer. Metodebok for utarbeidelse av nasjonale retningslinjer. Oslo: Helsedirektoratet, 2002.
Mednytt. www.mednytt.no
Nasjonalt kunnskapssenter for helsetjenesten. Slik oppsummerer vi forskning. Håndbok for Nasjonalt kunnskapssenter for helsetjenesten. 3. reviderte utg. Oslo: Nasjonalt kunnskapssenter for helsetjenesten, 2011.
Ringard Å, Mørland B, Røttingen JA. Åpne prosesser for prioritering. Tidsskr Nor Legeforen 2010; 130: 2264–6.
Nasjonalt råd for kvalitet og prioritering i helsetjenesten. Bruk av monoklonale antistoffer i behandling av metastatisk kolorektalcancer. Endelig vedtak. http://www.kvalitetogprioritering.no/Saker/Bruk+av+monoklonale+antistoffer+i+behandling+av+metasta tisk+kolorektalcancer.12213.cms.
Sullivan R, Peppercorn J, Sikora K et al. Delivering affordable cancer care in high-income countries. Lancet Oncology 2011; 12: 933–80.
Helse og omsorgsdepartementet. Nasjonal helse- og omsorgsplan (2010–2011). St. meld. nr. 16 (2010–2011). Oslo: helse og omsorgsdepartementet, 2011.
Guyatt GH, Oxman AD, Vist G, Kunz R, Falck-Ytter Y, Alonso-Coello P, Schünemann HJ, for the GRADE Working Group. Rating quality of evidence and strength of recommendations GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ 2008; 336; 924–926.
lenekristine.juvet@kunnskapssenteret.no
berit.morland@kunnskapssenteret.no
inn@kunnskapssenteret.no
marianne.klemp@kunnskapssenteret.no
john-arne.rottingen@kunnskapssenteret.no
Nasjonalt kunnskapssenter for helsetjenesten
Postboks 7004 St. Olavs plass
0130 Oslo
borghild.svorken@helsedir.no
hpa@helsedir.no
stein.kaasa@helsedir.no
Helsedirektoratet
Postboks 7000 St. Olavs plass
0130 Oslo
